【媒體報導】百朗克異軍突起 抗生素力退巴金森氏症
撰文、攝影/徐淨
>>本文經環球生技月刊授權轉載。
>>本文經環球生技月刊授權轉載。
中山醫學大學教授何應瑞發現,已在臨床使用超過30年的抗生素頭孢曲松(ceftriaxone)能夠促進神經細胞新生及回復其活性,今年初,美國FDA以28天火速通過其用於治療巴金森氏症的II期臨床試驗申請,國內TFDA也以罕見的23天審核通過。目前,臨床II期試驗正於多中心積極進行中。
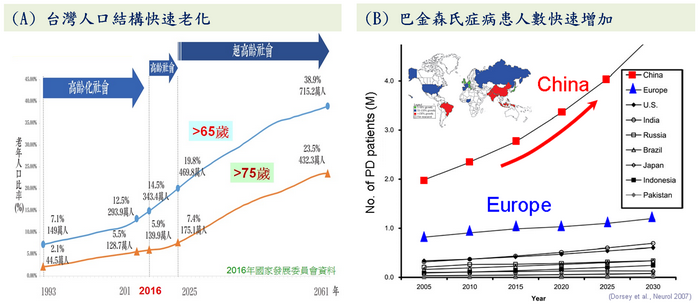
在安海瑟薇所主演的電影《愛情藥不藥》當中,才華洋溢、青春貌美的梅姬,年紀輕輕就被迫面臨失去自己肌肉控制的恐懼,而此疾病—巴金森氏症,更常見發生於老年人口,60歲以上盛行率約1%左右。
臺灣目前有20~30萬人口罹患程度不等的巴金森氏症,全球有近1,000萬人。隨著社會結構不斷趨向老齡化,患病趨勢不論地區皆不斷成長,影響了各國生產力及醫療負擔的加重。
臺灣目前有20~30萬人口罹患程度不等的巴金森氏症,全球有近1,000萬人。隨著社會結構不斷趨向老齡化,患病趨勢不論地區皆不斷成長,影響了各國生產力及醫療負擔的加重。
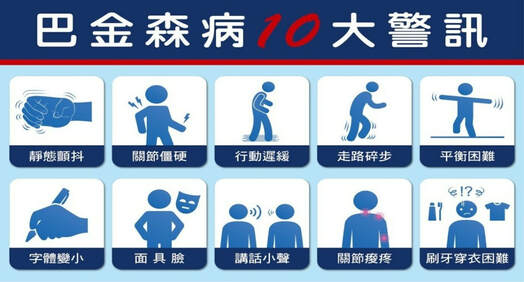
巴金森氏症起先3至5年會有愈來愈嚴重的震顫、肌肉僵硬、平衡不穩,而此疾病最可怕的,莫過於患者是頭腦清晰地面臨自己逐漸失能、癱瘓、失智、死亡。
國際間在神經退化性疾病藥物方面屢戰屢敗,不過,在今年年初,一家2017年剛成立的百朗克(BrainX),旗下巴金森氏症新藥C100火速通過美國FDA、臺灣TFDA審核通過II期臨床試驗,吸引了業內、國際間相當多的關注。
中山醫學大學教授何應瑞發現,已在臨床使用超過30年的抗生素頭孢曲松(Ceftriaxone, CEF)能夠促進神經細胞新生及回復其活性,而團隊在主要投資人瑞金生技集團總裁江文舜支持下成立BrainX。目前臨床團隊皆對試驗有信心,目標兩年內能完成II期臨床。
中山醫學大學教授何應瑞發現,已在臨床使用超過30年的抗生素頭孢曲松(Ceftriaxone, CEF)能夠促進神經細胞新生及回復其活性,而團隊在主要投資人瑞金生技集團總裁江文舜支持下成立BrainX。目前臨床團隊皆對試驗有信心,目標兩年內能完成II期臨床。
左多巴和深腦刺激解決不了的事
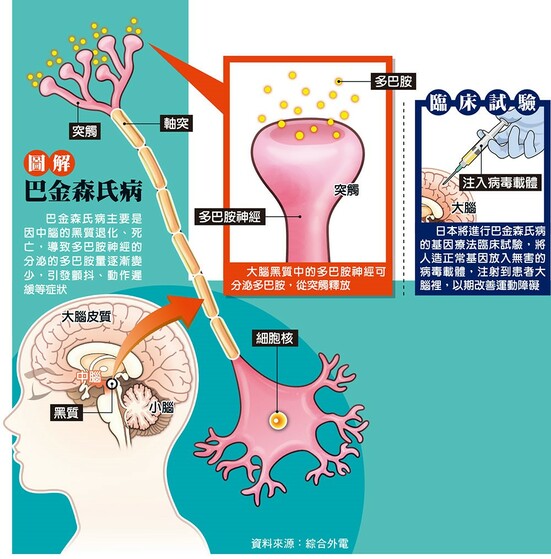
巴金森氏症最早的記錄在1817年,由醫師詹姆巴金森(James Parkinson)所描述。100多年後的1919年,俄羅斯神經科學家康斯坦丁特列季亞可夫(Konstantin Tretiakoff)釐清了此疾病的病理原因,發現是由於中腦黑質部的多巴胺神經系統退化所致。
巴金森氏症最早的記錄在1817年,由醫師詹姆巴金森(James Parkinson)所描述。100多年後的1919年,俄羅斯神經科學家康斯坦丁特列季亞可夫(Konstantin Tretiakoff)釐清了此疾病的病理原因,發現是由於中腦黑質部的多巴胺神經系統退化所致。
理解了致病因素,1960年代,左多巴(Levodopa)成為了直到今日都還廣泛使用的解決方案。左多巴為多巴胺前驅物,能穿越血腦屏障進入大腦,由多巴胺神經細胞轉化為多巴胺,緩解運動障礙症狀。
然而,左多巴並不能逆轉病情,多巴胺神經會持續衰退死亡,最終左多巴也無用武之地,持續退化的部位來到了海馬迴,高達八成的患者因此終將產生認知障礙,出現失智症狀(Parkinson’s Disease Dementia, PDD)。
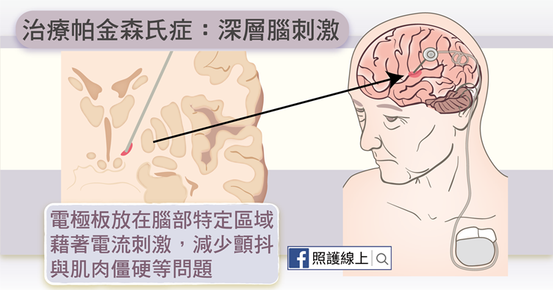
1997年,深腦刺激(Deep Brain Stimulation)被FDA有條件核准用於治療巴金森氏症患者,似乎終能達到在源頭視丘下核(Subthalamic Nucleus, STN)控制不正常放電的病根。然而,由於手術屬於不可逆、侵入性手段且所費不貲,此治療方式並非最好的方案。
然而,左多巴並不能逆轉病情,多巴胺神經會持續衰退死亡,最終左多巴也無用武之地,持續退化的部位來到了海馬迴,高達八成的患者因此終將產生認知障礙,出現失智症狀(Parkinson’s Disease Dementia, PDD)。
1997年,深腦刺激(Deep Brain Stimulation)被FDA有條件核准用於治療巴金森氏症患者,似乎終能達到在源頭視丘下核(Subthalamic Nucleus, STN)控制不正常放電的病根。然而,由於手術屬於不可逆、侵入性手段且所費不貲,此治療方式並非最好的方案。
「抗生素妙用,第一時間我也不敢確信」
長達5、60年以來,治療方案一直停留在左多巴與深腦刺激,巴金森氏症仍有偌大的醫療未滿。
這讓深諳神經心理科學並縱橫藥學背景,鑽研相關疾病多年的何應瑞,長年試圖找到該疾病治療的突破口。「我認為CEF將是神經退化性疾病治療領域的Game-Changer。」
抗生素頭孢曲松過去用於腦膜炎、肺炎、淋病等細菌感染,而團隊何以發現利用抗生素應用在神經疾病的治療呢?
何應瑞指出,所有神經退化性疾病雖有不同的致病機制,但都有一個共通點,那就是興奮性神經傳遞物質麩胺酸(Glutamate)的過量聚集,造成了神經毒性使神經元死亡。而麩胺酸的過度表達來自視丘下核的異常放電。
神經系統中的星狀膠細胞會負責回收這些麩胺酸,過去有美國研究團隊已發現,CEF能夠加速這個清除步驟。
「CEF用在神經疾病治療其實也並非首例,2012年有團隊使用CEF成功治癒孤兒疾病亞歷山大疾病。」
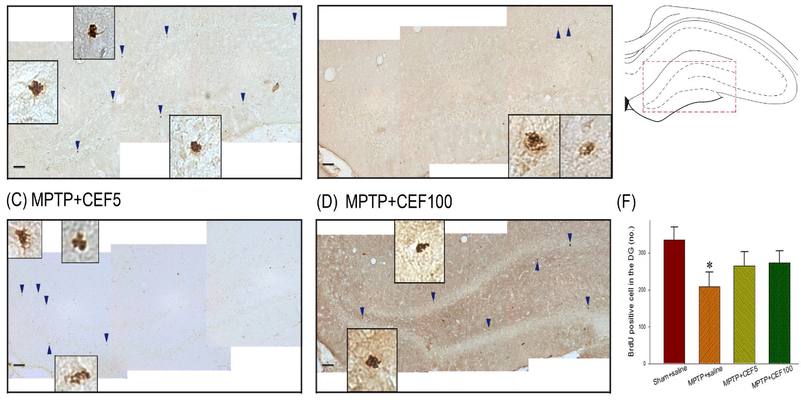
團隊在多次的小鼠實驗中,證實了CEF的治療機轉,針對病理三個核心進行各個擊破――包括清除麩胺酸;刺激神經新生以修復多巴胺和海馬迴――以消除運動及認知功能障礙,甚至可望從源頭視丘下核修復異常放電神經電位。
長達5、60年以來,治療方案一直停留在左多巴與深腦刺激,巴金森氏症仍有偌大的醫療未滿。
這讓深諳神經心理科學並縱橫藥學背景,鑽研相關疾病多年的何應瑞,長年試圖找到該疾病治療的突破口。「我認為CEF將是神經退化性疾病治療領域的Game-Changer。」
抗生素頭孢曲松過去用於腦膜炎、肺炎、淋病等細菌感染,而團隊何以發現利用抗生素應用在神經疾病的治療呢?
何應瑞指出,所有神經退化性疾病雖有不同的致病機制,但都有一個共通點,那就是興奮性神經傳遞物質麩胺酸(Glutamate)的過量聚集,造成了神經毒性使神經元死亡。而麩胺酸的過度表達來自視丘下核的異常放電。
神經系統中的星狀膠細胞會負責回收這些麩胺酸,過去有美國研究團隊已發現,CEF能夠加速這個清除步驟。
「CEF用在神經疾病治療其實也並非首例,2012年有團隊使用CEF成功治癒孤兒疾病亞歷山大疾病。」
團隊在多次的小鼠實驗中,證實了CEF的治療機轉,針對病理三個核心進行各個擊破――包括清除麩胺酸;刺激神經新生以修復多巴胺和海馬迴――以消除運動及認知功能障礙,甚至可望從源頭視丘下核修復異常放電神經電位。
實驗結果,在小鼠行為觀察到運動功能、短期記憶、辨識能力的恢復,組織切片、醫學成像(TRODAT、MRI)中觀察到神經密度提高以及活性的重生。
何應瑞表示,「第一時間看到神經細胞密度恢復的實驗結果,連我也難以相信,因為過去教科書告訴我們,能為神經退化做到的,最多只能減緩。」
但經過反覆驗證,臨床合作團隊皆有信心。目前探索型研究中已有幾個成功的參考案例,例如:高年73歲的巴金森氏症患者被建議需要進行DBS(深腦刺激)手術,但後來沒有選擇DBS,而是採用頭袍曲松CEF治療一年,運動功能、認知相關語言能力、心理指標皆有顯著改善,在醫學影像中也觀察到神經保護和恢復的成效。
何應瑞表示,「第一時間看到神經細胞密度恢復的實驗結果,連我也難以相信,因為過去教科書告訴我們,能為神經退化做到的,最多只能減緩。」
但經過反覆驗證,臨床合作團隊皆有信心。目前探索型研究中已有幾個成功的參考案例,例如:高年73歲的巴金森氏症患者被建議需要進行DBS(深腦刺激)手術,但後來沒有選擇DBS,而是採用頭袍曲松CEF治療一年,運動功能、認知相關語言能力、心理指標皆有顯著改善,在醫學影像中也觀察到神經保護和恢復的成效。
神經退化性疾病治療新星
研究成果廣受各界矚目,包括今年3月,於波蘭華沙舉行的神經學論證國際研討會上,響應熱烈;FDA通過臨床II期審核後,也有許多國際團隊主動前來尋求合作。
目前,在臺大醫院、高醫、中榮、中山醫學中心及美國已啟動多國多中心收案,預計募集106人受試者,收案資格需排除已裝設DBS的患者,因為深度腦電極會干擾藥物的效果。
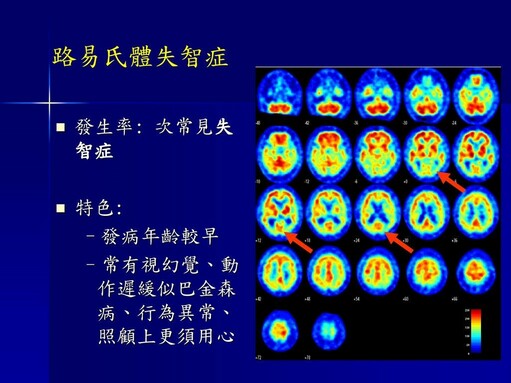
C100專利佈局也相當完整,包括臺灣、美國、澳洲、中國、日本等,近期也獲歐盟專利,以及全球第一項針對路易士體失智症(Dementia with Lewy Bodies, DLB)為適應症的專利申請也已通過。
研究成果廣受各界矚目,包括今年3月,於波蘭華沙舉行的神經學論證國際研討會上,響應熱烈;FDA通過臨床II期審核後,也有許多國際團隊主動前來尋求合作。
目前,在臺大醫院、高醫、中榮、中山醫學中心及美國已啟動多國多中心收案,預計募集106人受試者,收案資格需排除已裝設DBS的患者,因為深度腦電極會干擾藥物的效果。
C100專利佈局也相當完整,包括臺灣、美國、澳洲、中國、日本等,近期也獲歐盟專利,以及全球第一項針對路易士體失智症(Dementia with Lewy Bodies, DLB)為適應症的專利申請也已通過。
何應瑞感性地說,「現在協助臨床試驗的患者們,可能都等不到這個新藥上市了。但期待未來在診間,當醫師診斷出一個人罹患PDD時,還能放心地告訴他,『別擔心,我們有藥給你。』」
江文舜也表示,「百朗克雖只是一間年輕的小公司,以目前的成果來看,相信臨床試驗的成功只是時間的問題,必將集眾人之力,讓科學研究無後顧之憂。」
江文舜也表示,「百朗克雖只是一間年輕的小公司,以目前的成果來看,相信臨床試驗的成功只是時間的問題,必將集眾人之力,讓科學研究無後顧之憂。」